Analysis of Methods for Normalizing Lipid Profile and Blood Pressure in Patients with Chronic Coronary Syndromes
- Authors: Filina Z.V.1, Lityushkina M.I.1, Alayeva Z.G.1, Kiryukhin V.O.1, Dyrina M.M.1
-
Affiliations:
- National Research Mordovia State University
- Issue: Vol 1, No 3 (2025)
- Pages: 286-297
- Section: Internal medicine
- Submitted: 05.06.2025
- Accepted: 12.09.2025
- Published: 22.09.2025
- URL: https://medbiosci.ru/MedBiotech/article/view/295462
- DOI: https://doi.org/10.15507/3034-6231.001.202503.286-297
- EDN: https://elibrary.ru/jzugzh
- ID: 295462
Cite item
Full Text
Abstract
Introduction. Despite advancements in modern cardiology, cardiovascular diseases remain the leading cause of death in the Russian Federation and worldwide. A key predictor of these diseases is hyperlipidemia. Current treatment strategies involve increasingly aggressive lipid-lowering therapy to achieve target levels of low-density lipoprotein cholesterol and triglycerides. The aim of this study is a comprehensive investigation of the major risk factors for the development of ischemic heart disease and an analysis of the drug therapy used in patients with chronic coronary syndromes.
Materials and methods. We studied 85 outpatient medical records of patients with established diagnoses of “Stable exertional angina” and “Post-infarction cardiosclerosis” aged between 40 and 85 years (the mean age of participants was 65.27 (±1.02) years; 49 men and 36 women). Patients with acute coronary syndromes were not included in the study. The study was conducted through a retrospective analysis of outpatient medical records.
Results. Studying the processes of plaque formation in blood vessels (atherogenesis) and the influence of various risk factors (e.g., smoking, obesity, diabetes, arterial hypertension) helps to better understand the pathophysiology of the disease and develop effective preventive measures. The analysis revealed insufficient efficacy of the ongoing statin therapy in this patient group, as the target levels of low-density lipoprotein cholesterol were not achieved. Modern treatment methods include lifestyle modifications, dietary therapy, and the use of pharmacological agents (statins, ezetimibe, bile acid sequestrants, fibrates). However, the effectiveness of these approaches is limited, particularly in severe cases of familial hypercholesterolemia. Therefore, further research is necessary to develop new therapeutic strategies, such as PCSK9-inhibiting monoclonal antibodies and drugs that reduce cholesterol synthesis in the liver. The development of personalized treatment approaches based on individual patient characteristics (genotype, phenotype, comorbidities) will improve therapy efficacy and reduce drug side effects.
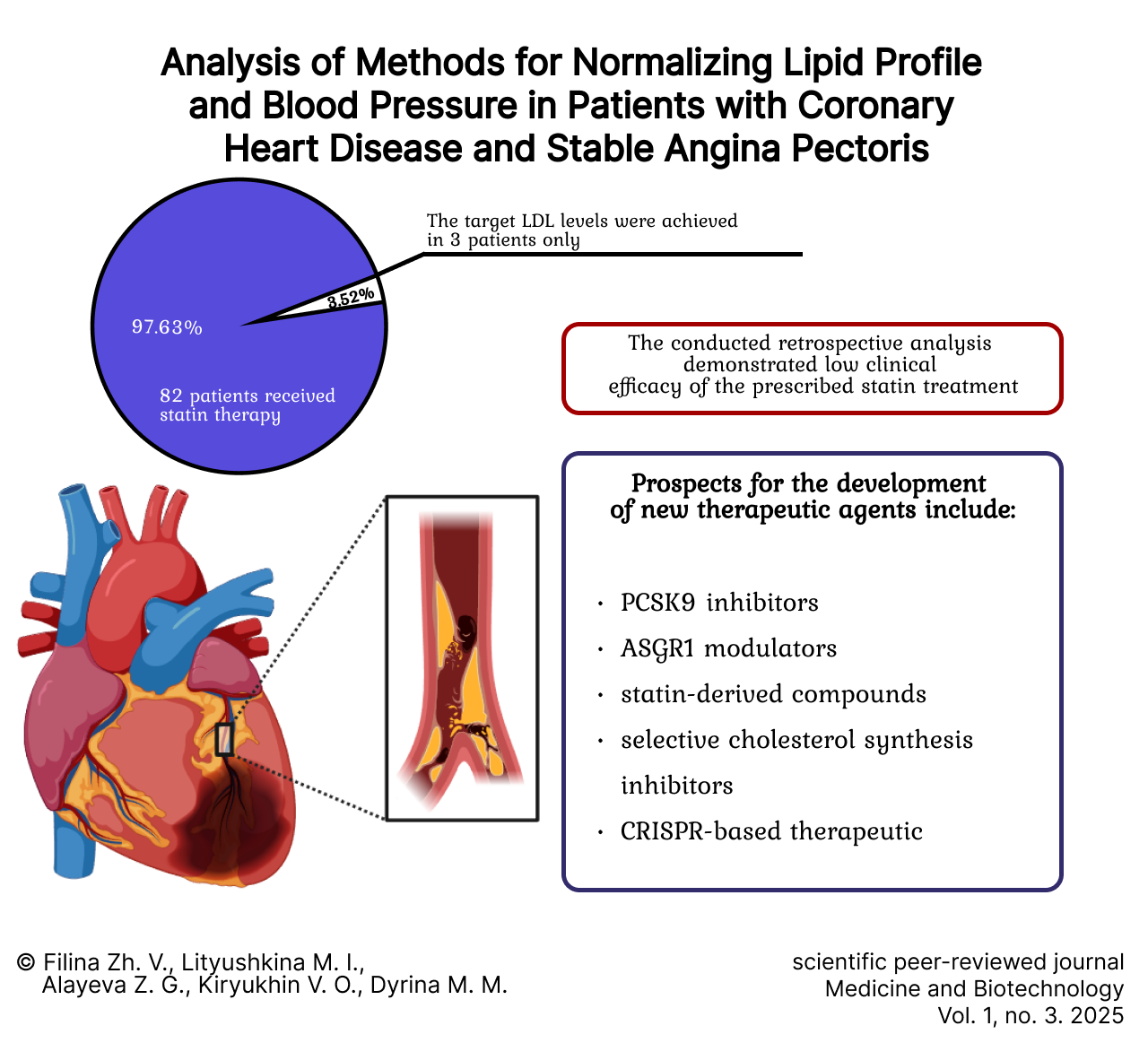
Discussion and conclusion. Analysis of retrospective data obtained from outpatient records revealed the treatment strategies employing lipid-lowering drugs (atorvastatin, rosuvastatin, simvastatin) used in the patients. Out of 85 patients, 82 (97.64%) received statins. Only 3 patients (3.52%) achieved the target levels of low-density lipoprotein cholesterol. The conducted retrospective analysis demonstrated the low clinical efficacy of the prescribed statin therapy. The prospects for developing new drugs to treat hypercholesterolemia are focused around several key areas: PCSK9 inhibitors (proprotein convertase subtilisin/kexin type 9 inhibitors), ASGR1 modulators (asialoglycoprotein receptor 1 modulators), statin derivatives, selective cholesterol synthesis inhibitors, and therapies using the “genomic scissors” technique (e.g., CRISPR-based approaches). The presented research perspectives create the prerequisites for developing an individualized management algorithm for each patient. This approach has the potential to significantly minimize the likelihood of adverse drug reactions and optimize the clinical outcomes of the treatment process.
Full Text
ВВЕДЕНИЕ
Стабильная стенокардия напряжения является одним из клинических фенотипов ишемической болезни сердца (ИБС), который характеризуюется преходящими ангинозными приступами сжимающего характера в области грудной клетки, обусловленными транзиторной дизадаптацией между оксигенационными требованиями миокарда и коронарной перфузией, особенно во время физической активности или психоэмоционального стресса. Этот тип составляет значимую долю в общей структуре заболеваемости ИБС, однако отмечается тенденция к уменьшению его распространенности. Несмотря на снижение частоты встречаемости новых случаев, показатель летальности от ИБС в Российской Федерации остается высоким, достигая уровня 328,5 на 100 тыс. населения. Ключевым патофизиологическим механизмом развития ИБС служит атеросклеротическая облитерация коронарных сосудов, что определяет необходимость модификации ключевых факторов риска, таких как гиперлипидемия, гипертензия, сахарный диабет и ожирение, в рамках стратегий вторичной профилактики.
В рекомендациях Европейского общества кардиологов (ESC) по диагностике и лечению хронических коронарных синдромов (2019 г.) был введен термин «хронические коронарные синдромы» (ХКС) для описания клинических проявлений ИБС в периоды стабильности, особенно предшествующие или следующие за острым коронарным синдромом (ОКС). ИБС определена как патологический процесс, характеризующийся накоплением необструктивных и обструктивных атеросклеротических бляшек в эпикардиальных артериях. На основе расширенных патофизиологических концепций ХКС принято считать ряд клинических проявлений или синдромов, возникающих вследствие структурных и/или функциональных изменений, связанных с хроническими заболеваниями коронарных артерий и/или микроциркуляции. Эти изменения могут привести к преходящему, обратимому несоответствию потребности миокарда в кровоснабжении, что приводит к гипоперфузии (ишемии), обычно (но не всегда) провоцируемой физической нагрузкой, эмоциями или другими стрессовыми ситуациями, и могут проявляться стенокардией, другими неприятными ощущениями в груди, одышкой или протекать бессимптомно. Несмотря на длительную стабильность, ХКС часто прогрессируют и могут дестабилизироваться в любой момент с развитием ОКС [1; 2].
Статины являются основными лекарственными препаратами для лечения атеросклероза благодаря своей способности снижать уровень холестерина липопротеинов низкой плотности (ХС ЛНП), что подтверждено многолетним опытом их использования [2; 3]. Комбинация статинов с эзетимибом и кумабами позволяет достичь целевых значений ХС ЛНП ниже 1,4 ммоль/л (< 55 мг/дл), которые рекомендованы ESC [1; 2; 4]. Однако остаются сложности в достижении оптимального контроля липидов, особенно при монотерапии, что требует улучшения терапевтических подходов [3]. Для достижения более значительного снижения концентрации ХС ЛНП, особенно у пациентов с повышенным риском сердечно-сосудистых патологий, в клинической практике широко применяются высокоинтенсивные препараты (розувастатин и аторвастатин), а также моноклональные антитела – ингибиторы пропротеинконвертазы субтилизина / кексина типа 9 (PCSK9), участвующие в процессе взаимодействия молекул ХСм ЛНП с рецепторами [2].
Одновременно с этим в клинической практике укрепляется концепция комбинированной гиполипидемической терапии, эффективность которой была окончательно подтверждена в исследовании IMPROVE-IT, демонстрирующем преимущества сочетания симвастатина с эзетимибом [5]. Подобно фиксированным комбинациям в терапии гипертонии, использование комбинированных липидснижающих средств может трансформировать подходы к начальному лечению, ускоряя достижение целевых уровней и уменьшая риски у пациентов с высокой вероятностью осложнений. Данные исследований демонстрируют, что фиксированная комбинация статинов с эзетимибом у лиц с крайне высоким риском снижает риск на 9 % по сравнению с обычными сочетаниями препаратов [6; 7].
Одной из ключевых проблем остается недостаточная диагностика нарушений липидного обмена у пациентов до возникновения первого сердечно-сосудистого события [8]. Проведенный исследователями метаанализ 25 рандомизированных клинических исследований (РКИ) (47 тысяч пациентов, принимавших статины) и 22 РКИ (118 тысяч пациентов, получавших комбинированную терапию) показал, что снижение уровня ХС ЛНП уменьшает риск сердечно-сосудистых событий у групп высокого риска [9].
В НИИ медицинских проблем Севера (2018–2019 гг.) исследовали 1 671 пациента с ХКС (770 мужчин, 901 женщина). Гиполипидемические препараты принимали 51,4 %, преимущественно в виде монотерапии статинами (99,2 %; наиболее часто аторвастатин – 74,6 %). Комбинированная терапия использовалась редко (0,8 %). Только 16,3 % участников достигло целевого уровня ХС ЛНП <1,8 ммоль/л, 6,5 % – <1,4 ммоль/л. Статины высокой интенсивности показали лучшие результаты: 37,5 % достигли уровня <1,8 ммоль/л, 23,9 % – <1,5 ммоль/л, 20,7 % – <1,4 ммоль/л. Необходимость расширения применения высокоинтенсивных статинов и комбинированной терапии очевидна [10].
Исследователи из Университета Монаша (Австралия) провели систематический обзор 44 работ, выявивший сравнимую эффективность различных статинов в снижении ХС ЛНП. В исследовании участвовали 290 пациентов из 19 корейских центров. Их разделили на четыре группы: A5E (аторвастатин 5 мг + эзетимиб 10 мг), E (эзетимиб 10 мг), A5 (аторвастатин 5 мг) и A10 (аторвастатин 10 мг). Обследования проводились трижды с интервалом в 4 недели. Основная цель исследования заключалась в оценке изменения уровня ХС ЛНП через 8 недель [11]. Все статины имели аналогичные побочные эффекты, частота которых возрастала при увеличении дозировок.
В открытое рандомизированное исследование отсутствия меньшей эффективности было включено население с атеросклеротическими сердечно-сосудистыми заболеваниями из клиник Южной Кореи, произвольно распределенное поровну между группами комбинированной терапии розувастатином 10 мг и эзетимибом 10 мг и монотерапии розувастатином 20 мг. Исследование включало 3 780 пациентов, разделенных на две группы – группу комбинированной терапии и группу монотерапии высокодозовыми статинами. Через три года наблюдения концентрации ХС ЛНП ниже целевого уровня (<1,8 ммоль/л) наблюдались у значительно большего числа участников первой группы (около 73%) по сравнению со второй группой (примерно 58%) [12].
Монотерапия статинами не всегда позволяет достигнуть целевого уровня липидов. Комбинация эзетимиба с низкой дозой аторвастатина эффективнее снижает уровень ХС ЛНП, чем умеренная доза аторвастатина, обеспечивая лучший контроль липидного профиля у пациентов с низким и средним риском [13; 14; 15].
Цель исследования – комплексное выявление основных факторов риска развития ИБС и проведение фармакоэпидемиологического анализа лекарственной терапии, применяемой у пациентов с подтвержденным диагнозом ИБС, включая стабильную стенокардию напряжения и постинфарктный кардиосклероз (ПИКС).
МАТЕРИАЛЫ И МЕТОДЫ
Объектом изучения являлись амбулаторные карты 85 пациентов с верифицированными диагнозами «Стабильная стенокардия напряжения» и «Постинфарктный кардиосклероз» в возрасте от 40 до 85 лет, средний возраст составил 65,27 (±1,02) гг., среди которых 49 мужчин, 36 женщин. Критерии включения в исследование основывались на наличии установленного диагноза «Стабильная стенокардия напряжения», пациенты с острыми формами ИБС были исключены из анализа. Изучали степень выраженности и длительности стенокардитических атак, идентифицировали факторы риска установленных заболеваний, сопутствующая патология, а также проводили интерпретацию результатов лабораторно-диагностического обследования крови, включая показатели липидограммы: ХС, триглицериды (ТГ), ХС ЛНП, ХС липопротеинов высокой плотности (ХС ЛВП); уровни трансаминаз (ммоль/л). Регистрировались данные давления крови (ДК) и частоты сердечных сокращений (ЧСС).
Статистический анализ проведен с использованием программ Microsoft Office Excel 2016 для Windows 10, рассчитывали количественные данные, имеющие нормальное распределение – среднее арифметическое (М) и стандартное отклонение (SD). Достоверность различий проверялась с помощью t-критерия Стьюдента.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
У участников исследования средняя длительность заболевания стенокардией (стенокардитических атак) составила 6,52 года. 46 пациентов ранее перенесли инфаркт миокарда. Систолическая хроническая сердечная недостаточность (ХСН) наблюдалась у 7 пациентов, диастолическая ХСН была выявлена у 52 пациентов (табл. 1).
Таблица 1. Клинико-демографическая характеристика пациентов
Table 1. Clinical and demographic characteristics of the patients
Показатели / Indicators | Всего участников (n=85) / Total participants (n=85) | Мужчины (n = 49) / Men (n = 49) | Женщины (n = 36) / Women (n = 36) |
Возраст, лет / Age, years | 65,27 (±1,02) | 62,57 (±1,23) | 68,94 (±1,54)* |
ФК стенокардии / Grade of effort angina severity II III | 33 (38,82 %) 52 (61,18 %) | 17 (34,69 %) 32 (65,31 %) | 16 (44,44 %) 20 (55,56 %) |
Давность стенокардии, лет / Duration of angina, years | 6,52 (±0,94) | 5,72 (±1,04) | 6,78 (±1,24) |
ПИКС / PICS | 46 (54,12 %) | 26 (53,06 %) | 20 (55,56 %) |
ХСН систолическая / Systolic CHF | 7 (8,24 %) | 4 (8,16 %) | 3 (8,33 %) |
ХСН диастолическая / Diastolic CHF | 52 (61,18 %) | 30 (61,22 %) | 22 (61,11 %) |
Примечания: * – достоверность различий в сравнении с показателями мужчин (p <0,05),
ФК – функциональный класс, ПИКС – постинфарктный кардиосклероз, ХСН – хроническая сердечная недостаточность
Notes: * – the significance of differences in comparison with the indicators of men (p <0.05),
FC – functional class, PICS – postinfarction cardiosclerosis, CHF – chronic heart failure
Источник: здесь и далее таблицы составлены авторами статьи
Source: here and further all tables are compiled by the authors of the article
У участников исследования были выявлены следующие факторы риска развития ИБС: артериальная гипертензия (98 %), ожирение и избыточный вес (86 %), гиперхолестеринемия (37 %) и сахарный диабет (15 %).
Из 85 респондентов 83 пациента (97,65 %) получали гиполипидемическую терапию статинами (табл. 2) с целью снижения уровня ХС ЛНП. Полученные ретроспективные данные позволили уточнить назначенные пациентам лекарственные препараты и результат их действия. При назначенных дозах препаратов целевой уровень ХС ЛНП был достигнут только у 3 пациентов (3,61 %).
Таблица 2. Суточные дозы статинов, назначенные пациентам
Table 2. Daily doses of statins prescribed to patients
Лекарственный препарат / Medicinal product | Доза (М), мг / Dose (M), mg |
Аторвастатин / Atorvastatin | 16,35 (±0,67) |
Розувастатин / Rosuvastatin | 12,08 (±0,99) |
Симвастатин / Simvastatin | 16,67 (±3,33) |
Низкую эффективность гиполипидемической терапии можно связать с несколькими причинами: низким комплаенсом [16]; недостаточной дозировкой [2]; низким качеством лекарственных средств [17; 18].
У всех пациентов оценивалась активность аланиновой и аспарагиновой трансаминаз в сыворотке крови [19]. Повышенные значения (в 3 и 1,5 раза выше нормы) наблюдались у одного пациента с сопутствующим гепатитом, у 84 пациентов показатели находились в пределах референсных значений [1; 2].
Антиангинальная терапия включала бета-блокаторы (ББ) и недигидропиридиновые блокаторы кальциевых каналов (не-дпБКК), уменьшающие потребность миокарда в кислороде через отрицательный хронотропный и инотропный эффект [1; 5]. Дозировка корректировалась до достижения ЧСС менее 60 уд /мин в покое при синусовом ритме.
В исследовании 68 (80 %) пациентов получали ББ, 4 (4,71 %) пациента – не-дпБКК. 13 участников (15,29 %) не получали препараты, снижающие ЧСС (табл. 3).
Таблица 3. Средние дозы бета-блокаторов
Table 3. Average doses of beta-blockers
Лекарственный препарат / Medicinal product | Доза (М), мг / Dose (M), mg |
Бисопролол / Bisoprolol | 3,69 (±0,21) |
Метопролол SR / Metoprolol SR | 44,11 (±4,56) |
Карведилол / Carvedilol | 12,5 (±4,42) |
Небиволол / Nebivоlol | 4,16 (±0,83) |
Целевой уровень ЧСС в покое достигался только у 31 (36,47 %) пациента.
Из других антиангинальных препаратов 26 пациентам (30,59 %) назначались пролонгированные нитраты, 8 пациентам (9,41 %) – триметазидин.
Анализ последнего измерения ДК выявил достижение целевого уровня лишь у 36 пациентов (42,35 %). У 35 (41,18 %) участников уровень ДК был выше нормы, что свидетельствовало о недостаточной ДК-снижающей терапии, а у 14 (16,47 %) больных отмечались признаки гипотензии (АД < 100/60 мм рт. ст.), что указывало на избыточность ДК-снижающей терапии.
Антитромбоцитарная терапия назначалась 78 пациентам (91,76 %), в основном – ацетилсалициловая кислота, 4 пациента получали клопидогрел. Семь пациентов (8 %) не принимали эти препараты из-за противопоказаний.
ОБСУЖДЕНИЕ И ЗАКЛЮЧЕНИЕ
ХС ЛНП является модифицируемым фактором риска, связанным с сердечно-сосудистыми заболеваниями. Клинические испытания убедительно доказывают пользу снижения уровня ЛНП с помощью статинов для сердечно-сосудистой системы. Поэтому международные рекомендации предлагают снижать уровень ХС ЛНП до целевых значений, чтобы уменьшить риск сердечно-сосудистых катастроф. Однако эти цели достигаются лишь у меньшинства пациентов. Согласно данным таких реестров, как исследование EUROASPIRE V в 27 европейских странах, уровень ХС ЛНП ниже 1,81 ммоль/л достигается менее чем у трети пациентов с очень высоким сердечно-сосудистым риском [20]. При этом, согласно рекомендациям ESC, для пациентов, у которых в течение двух лет на фоне максимально переносимой терапии статинами возникает второе сосудистое событие, целевым можно считать еще более низкий уровень ХС ЛНП – < 1,0 ммоль/л (< 40 мг/дл) [2].
Проведенный ретроспективный анализ амбулаторных карт выявил низкую клиническую эффективность статинотерапии у большинства пациентов с дислипидемией. Полученные данные подчеркивают необходимость дальнейшей персонализации гиполипидемической терапии и поиска прогностически значимых биомаркеров, определяющих чувствительность организма к статинам. Результаты исследования обосновывают целесообразность углубленного изучения механизмов устойчивости к препаратам класса статинов и разработку принципиально новых терапевтических подходов для достижения оптимального контроля липидных нарушений.
Согласно рекомендациям ESC, перспективными являются разработки новых препаратов для лечения гиперхолестеринемии: ингибиторов PCSK9, модуляторов асиалогликопротеинового рецептора 1, статиновых производных, селективных ингибиторов синтеза холестерина, терапии методикой «геномных ножниц» (CRISPR-терапия) [2].
Уже имеются данные об эффективности применения моноклональных антител (мАТ) к PCSK9 в сочетании со статинами в виде выраженного снижения концентрации ХС ЛНП у больных с высоким сердечно-сосудистым риском и у пациентов с семейной гиперхолестеринемией. При этом одним из недостатков мАТ является необходимость введения препаратов (эволокумаб, алирокумаб) каждые 2 или 4 недели для снижения уровней циркулирующего PCSK9 и ХС ЛНП. Поэтому в качестве новых методов лечения для супрессии уровня PCSK9 разрабатываются средства анти-РНК-терапии: антисмысловые олигонуклеотиды и малые интерферирующие РНК (siRNA), конъюгированные с N-ацетилгалактозамином – инклисиран, который может вводиться каждые 6 месяцев после первоначального 3-месячного интервала дозирования [21].
Представленные исследовательские результаты создают предпосылки для разработки персонализированного алгоритма ведения пациента, позволяющего минимизировать вероятность побочных эффектов и снизить стоимость медикаментозной терапии за счет оптимизации кратности применения, достичь целевых уровней липидного профиля и давления крови.
About the authors
Zhanna V. Filina
National Research Mordovia State University
Author for correspondence.
Email: filina.zhanna79@gmail.com
ORCID iD: 0009-0000-5520-464X
Assistant Professor of Propaedeutics of Internal Diseases
Russian Federation, 68 Bolshevistskaya St., Saransk 430005Marina I. Lityushkina
National Research Mordovia State University
Email: litjushkina@rambler.ru
ORCID iD: 0000-0002-6098-4158
SPIN-code: 5068-8910
Cand.Sci. (Med.), Associate Professor of the Department of Propaedeutics of Internal Diseases
Russian Federation, 68 Bolshevistskaya St., Saransk 430005Zinaida G. Alayeva
National Research Mordovia State University
Email: alaeva1959@bk.ru
ORCID iD: 0009-0006-8991-1020
Assistant of the Department of Propaedeutics of Internal Diseases
Russian Federation, 68 Bolshevistskaya St., Saransk 430005Vadim O. Kiryukhin
National Research Mordovia State University
Email: ko4ka163@yandex.ru
ORCID iD: 0009-0001-0383-4671
Assistant of the Department of Propaedeutics of Internal Diseases
Russian Federation, 68 Bolshevistskaya St., Saransk 430005Marina M. Dyrina
National Research Mordovia State University
Email: mari.dyrina@yandex.ru
ORCID iD: 0009-0005-9317-9680
Undergraduate Student, Medical Institute
Russian Federation, 68 Bolshevistskaya St., Saransk 430005References
- Knuuti J., Wijns W., Saraste A., Capodanno D., Barbato E., Funck-Brentano C. et al.; ESC Scientific Document Group. 2019 ESC Guidelines for the Diagnosis and Management of Chronic Coronary Syndromes. European Heart Journal. 2020;41(3):407–477. https://doi.org/10.1093/eurheartj/ehz425
- Vrints C., Andreotti F., Koskinas K.C., Rossello X., Adamo M., Ainslie J. et al.; ESC Scientific Document Group. 2024 ESC Guidelines for the Management of Chronic Coronary Syndromes. European Heart Journal. 2024;45(36):3415–3537. https://doi.org/10.1093/eurheartj/ehae177
- Susekov V.A. Modern Algorithms for Statin Therapy. Russian Journal of Cardiology. 2023;28(10):5594. (In Russ., abstract in Eng.). https://doi.org/10.15829/1560-4071-2023-5594
- Karpov Yu.A. Efficacy and Safety of Achieving Novel Low-density Lipoprotein Cholesterol Target Levels: the Role of Combination Therapy. Atmosphere. Cardiology News. 2021;(2):3–11. (In Russ., abstract in Eng.). https://doi.org/10.24412/2076-4189-2021-12382
- Gurevich V.S., Solodovnikov A.G., Manko K.S., Timoshina E.V. The Efficacy of Ezetimibe and Statin Combination Therapy Compared to Statin Monotherapy: a Systematic Review and Meta-analysis of Observational Trials. Atmosphere. Cardiology News. 2023;3:33–46. (In Russ., abstract in Eng.). https://doi.org/10.24412/2076-4189-2023-13015
- Parati G., Kjeldsen S., Coca A., Cushman W.C., Wang J. Adherence to Single-Pill Versus Free-Equivalent Combination Therapy in Hypertension: A Systematic Review and Meta-Analysis. Hypertension. 2021;77(2):692–705. https://doi.org/10.1161/НYPERTENSIONAHA.120.15781
- Katzmann J.L., Sorio-Vilela F., Dornstauder E., Fraas U., Smieszek T., Zappacosta S. et al. Non-statin Lipid-lowering Therapy over Time in Very-high-risk Patients: Effectiveness of Fixed-dose Statin / Ezetimibe Compared to Separate Pill Combination on LDL-C. Clinical Research in Cardiology. 2022;111(3):243–252. https://doi.org/10.1007/s00392-020-01740-8
- Resolution of the National Scientific Council of Experts. Actual Questions of Intensification of Lipid-lowering therapy. Journal of Atherosclerosis and Dislipidemias. 2022;1(46):64–70. (In Russ.). URL: https://jad.noatero.ru/index.php/jad/article/view/360 (accessed: 25.05.2025).
- Goldstein L.B., Toth P.P., Dearborn-Tomazos J.L., Giugliano R.P., Hirsh B.J., Peña J.M.; American Heart Association Council on Arteriosclerosis, Thrombosis and Vascular Biology; Council on Cardiovascular and Stroke Nursing; Council on Peripheral Vascular Disease; and Stroke Council. Aggressive LDL-C Lowering and the Brain: Impact on Risk for Dementia and Hemorrhagic Stroke: a Scientific Statement from the American Heart Association. Arteriosclerosis, Thrombosis and Vascular Biology. 2023;43(10):e404–442. https://doi.org/10.1161/ATV.0000000000000164
- Gogolashvili N.G., Yaskevich R.A. Effectiveness of Lipidlowering Therapy in Outpatients with Coronary Artery Disease Living in a Large Industrial Center of Eastern Siberia. Cardiovascular Therapy and Prevention. 2021;20(8):82–90. (In Russ., abstract in Eng.). https://doi.org/10.15829/1728-8800-2021-3135
- Jaam M., Al-Naimi H.N., Haddad M.M., Abushanab D., Al-Badriyeh D. Comparative Efficacy and Safety among High-intensity Statins. Systematic Review and Meta-Analysis. Journal of Comparative Effectiveness Research. 2023;12(3):e220163. https://doi.org/10.57264/cer-2022-0163
- Lee S.A., Hong S.J., Sung J.H., Kim K.S., Kim S.H., Cho J.M. et al. Effectiveness of Low-intensity Atorvastatin 5 mg and Ezetimibe 10 mg Combination Therapy Compared with Moderate-intensity Atorvastatin 10 mg Monotherapy: A Randomized, Double-blinded, Multi-center, Phase III Study. Medicine (Baltimore). 2023;102(47):e36122. https://doi.org/10.1097/MD.0000000000036122
- RACING investigators; Kim B.K., Hong S.J., Lee Y.J., Hong S.J., Yun K.H., Hong B.K. et al. Long-term Efficacy and Safety of Moderate-intensity Statin with Ezetimibe Combination Therapy versus High-intensity Statin Monotherapy in Patients with Atherosclerotic Cardiovascular Disease (RACING): A Randomised, Open-label, Non-inferiority Trial. The Lancet. 2022;400(10349):380–390. https://doi.org/10.1016/S0140-6736(22)00916-3
- Ezhov M.V., Chubykina U.V., Dmitriev V.A. Difficulties in Achieving Target Levels of Low Density Lipoproteid Cholesterol in Patients with Atherosclerotic Cardiovascular Diseases in Real Clinical Practice. Journal of Atherosclerosis and Dyslipidaemias. 2023;4(53):27–34. (In Russ., abstract in Eng.). https://doi.org/10.34687/2219-8202.JAD.2023.04.0003
- Pracoń R., Demkow M., Anthopolos R., Mazurek T., Drożdż J., Witkowski A. et al. Optimal Medical Therapy in Patients with Stable Coronary Artery Disease in Poland: the ISCHEMIA Trial Experience. Polish Archives of Internal Medicine. 2021;131(11):16100. https://doi.org/10.20452/pamw.16100
- Cha J.J., Hong S.J., Kim J.H., Lim S., Joo H.J., Park J.H. et al. Effect of Rosuvastatin 20 mg Versus Rosuvastatin 5 mg Plus Ezetimibe on Statin Side-effects in Elderly Patients with Atherosclerotic Cardiovascular Disease: Rationale and Design of a Randomized, Controlled SaveSAMS Trial. American Heart Journal. 2023;261:45–50. https://doi.org/10.1016/j.ahj.2023.03.002
- Kovaleva K.A., Nemyatykh O.D., Okovityi S.V. Patient Compliance with Medical Recommendations: Realities and Perspectives. Therapy. 2025;11(2):137–148. (In Russ., abstract in Eng.). https://dx.doi.org/10.18565/therapy.2025.2.137-148
- Martsevich S. Yu., Kutishenko N. P., Voronina V. P., Ginzburg M. L., Suvorov A. Yu. Generics Statins: are All so Easy with Evidence of Clinical Equivalence? The Clinician. 2012;6(2):54–58. (In Russ., abstract in Eng.). https://doi.org/10.17650/1818-8338-2012-6-2-54-58
- Chaulin A.M. The Main Side Effects of Statins in Clinical Practice. Journal of Clinical Practice. 2022;13(2):98–107. (In Russ., abstract in Eng.). https://doi.org/10.17816/clinpract108076
- Kotseva K., De Backer G., De Bacquer D., Ryden L., Hoes A., Grobbee D. et al. Lifestyle and Impact on Cadiovascular Risk Factor Control in Coronary Patients across 27 Countries: Results from the European Society of Cardiology ESC-EORP EUROASPIRE V Registry. European Journal of Preventive Cardiology. 2019;26(8):824–835. https://doi.org/10.1177/2047487318825350
- Santos R.D., Rocha V.Z. Cholesterol Lowering with Inclisiran: A New Chapter in the PCSK9 Story Book. European Heart Journal. 2023;44(2):139–141. https://doi.org/10.1093/eurheartj/ehac656
Supplementary files