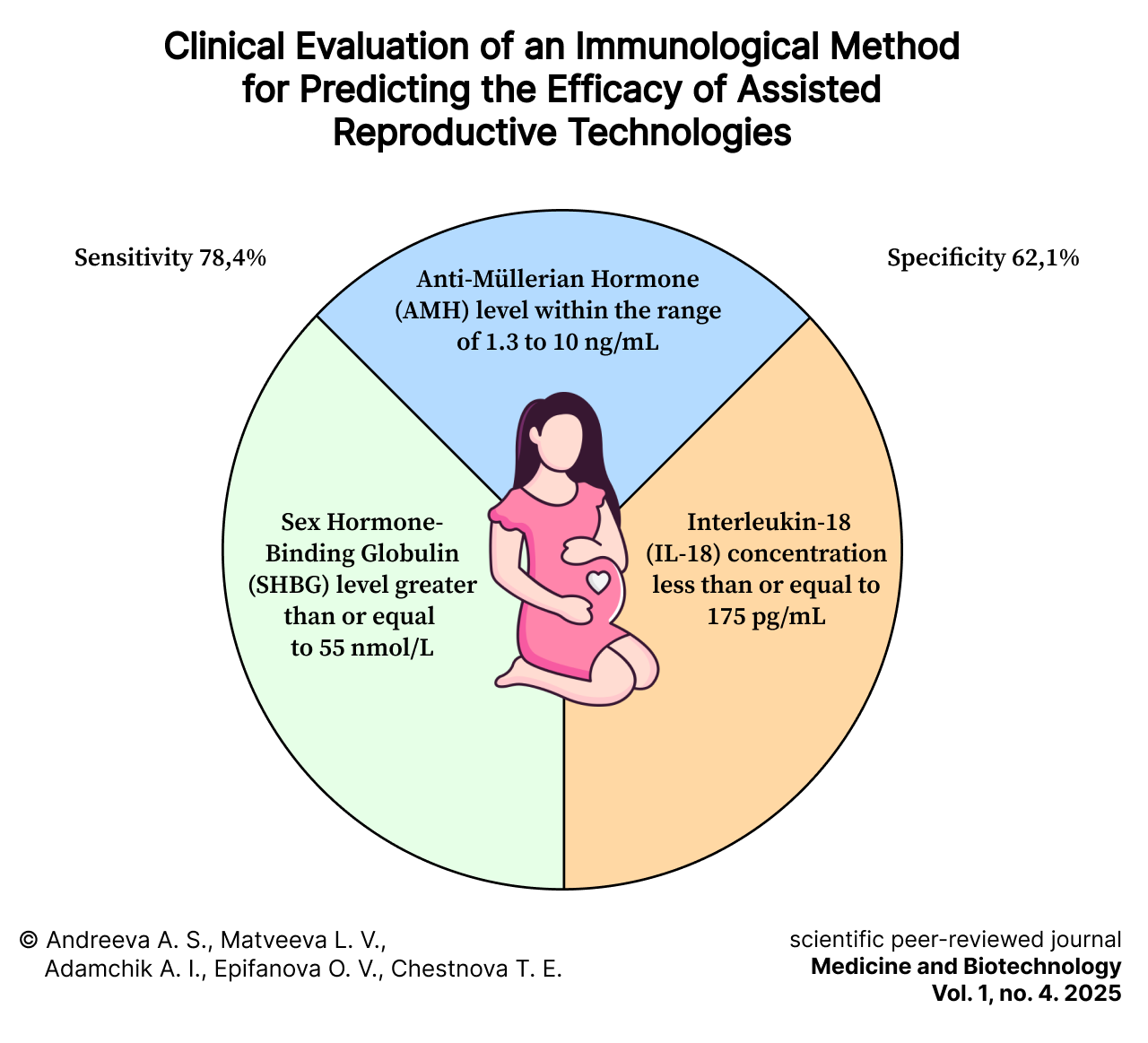
Clinical Evaluation of an Immunological Method for Predicting the Efficacy of Assisted Reproductive Technologies
- Authors: Andreeva A.S.1, Matveeva L.V.1, Adamchik A.I.2, Epifanova O.V.2, Chestnova T.E.2
-
Affiliations:
- National Research Mordovia State University
- Mordovia Republican Central Clinical Hospital
- Issue: Vol 1, No 4 (2025)
- Pages: 402-408
- Section: A case from clinical practice
- Submitted: 02.11.2025
- Accepted: 11.12.2025
- Published: 22.12.2025
- URL: https://medbiosci.ru/MedBiotech/article/view/349518
- DOI: https://doi.org/10.15507/3034-6231.001.202504.402-408
- EDN: https://elibrary.ru/fvlqrx
- ID: 349518
Cite item
Full Text
Abstract
Introduction. Infertility in marriage is a relevant medical and social problem in many countries worldwide, for which assisted reproductive technologies are actively used. The effectiveness of infertility treatment depends on a number of factors. The study and correction of immune parameters in reproductive medicine may contribute to reducing the rate of population infertility. The aim of this study is to conduct a clinical trial of a method for the immunological prediction of the effectiveness of assisted reproductive technologies.
Materials and methods. The method was trialed on 80 women with primary infertility, aged 19 to 47, prior to the use of assisted reproductive technologies. During the initial consultation, after obtaining informed consent, a blood sample was collected from the women, and serum was separated. The serum levels of Anti-Müllerian Hormone, Interleukin-18, and Sex Hormone-Binding Globulin were determined by enzyme-linked immunosorbent assay.
Results. Analysis of changes in serum levels of the studied parameters revealed variations dependent on female fertility status. The detection model based on a combination of these parameters for predicting pregnancy onset demonstrated a sensitivity of 78.4% and a specificity of 62.1%.
Discussion and сonclusion. Successful pilot testing of a method for the immunological prediction of the efficacy of assisted reproductive technologies in a cohort of women with primary infertility indicates its potential for use in immunodiagnostics, personalized assessment of pregnancy chances, and evaluation of the advisability of in vitro fertilization.
Full Text
ВВЕДЕНИЕ
Бесплодие в браке является актуальной медико-социальной проблемой в связи с низким естественным приростом населения. По данным Всемирной организации здравоохранения, каждый шестой человек в мире страдает от бесплодия1. Ведущей тактикой лечения бесплодия является применение вспомогательных репродуктивных технологий (ВРТ), из которых чаще проводится процедура экстракорпорального оплодотворения преовуляторных фолликулов и перенос дробящихся эмбрионов в полость матки (ЭКО). Эффективность ЭКО составляет примерно 37–39 % наступивших вследствие применения ВРТ беременностей. Низкая частота наступления беременности в программах ЭКО отмечается у женщин позднего репродуктивного возраста, что обусловлено снижением овариального резерва и качества ооцитов [1; 2].
В последние годы большое внимание уделяется изучению иммунных параметров при физиологическом и осложненном течении беременности, невынашивании, бесплодии. Для иммунологического прогнозирования эффективности применения ВРТ был разработан способ, использование которого актуально в репродуктивной медицине [3].
Цель работы – клиническая апробация способа иммунологического прогнозирования эффективности применения ВРТ.
МАТЕРИАЛЫ И МЕТОДЫ
Предиктивную оценку показателей проводили в ходе когортного проспективного наблюдения на 80 женщин с первичным бесплодием в возрасте от 19 до 47 лет перед проведением процедур ВРТ в отделении вспомогательных репродуктивных технологий Перинатального центра Мордовской республиканской центральной клинической больницы. Исследование одобрено Локальным этическим комитетом Медицинского института Национального исследовательского Мордовского государственного университета (протокол № 123 от 30.01.2024 г.). Диагноз определяли на основании клинико-анамнестических данных, результатов ультразвукового исследования (УЗИ) матки и придатков, молочных желез. Критериями исключения из исследования служили: получение иммунотропных лекарственных средств, проведение вакцинации и наличие острых инфекционных заболеваний в течение 1 месяца и менее до начала исследования. После применения ВРТ обследуемых женщин распределяли в группы сравнения. 1 группу составили женщины с наступившей беременностью (n = 51), 2 группу – женщины с ненаступившей беременностью (n = 29). Статистически значимых возрастных межгрупповых различий не выявлено.
При первичном обращении до применения ВРТ при получении информированного согласия у женщин проводили забор 7 мл крови в утренние часы натощак из кубитальной вены в пробирку с активатором свертывания, отделяли сыворотку при центрифугировании на скорости 1500 об/мин в течение 10–12 мин.
Содержание в сыворотке крови антимюллерова гормона (АМГ), интерлейкина (IL)-18 и секс-стероид-связывающего глобулина (ССГ) определяли путем иммуноферментного анализа с использованием тест-систем производства ООО «ХЕМА» и АО «ВЕКТОР-БЕСТ». Выбор комбинации параметров патогенетически обоснован [3].
Согласно методу, описанному в патенте на изобретение, при комбинации значений:
– АМГ от 1,3 до 10 нг/мл включительно;
– IL-18 ≤ 175 пг/мл;
– ССГ ≥ 55 нмоль/л прогнозировали благоприятный исход применения ВРТ [3].
При статистической обработке результаты представляли в виде медианы (Me), 1 квартиля (Q1), 3 квартиля (Q3). Достоверными считали межгрупповые различия при уровне значимости (р) < 0,05.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Анализ сывороточных уровней АМГ, IL-18 и ССГ у обследованных женщин выявил изменения их содержания, зависящие от фертильности (таблица).
Таблица. Сывороточные уровни параметров у обследованных женщин
Table. Serum levels of parameters in the examined women
Показатели / Parameters | 1 группа (n = 51) / | 2 группа (n = 29) / | |
АМГ, нг/мл / AMH, ng/ml | Me [Q1; Q3] | ||
5–95 ‰ | 1,3–10 | 2,7–13,5 | |
IL-18, пг/мл / IL-18, pg/ml | Me [Q1; Q3] | 120 [100; 140] | 176 [145; 267] * |
5–95 ‰ | 68–175 | 132–325 | |
ССГ, нмоль/л / SSBG, nmol/l | Me [Q1; Q3] | 40 [27; 55] | 28 [22; 36] * |
5–95 ‰ | 21–82 | 18–54 | |
Примечания: *– отличия от 1 группы при р < 0,05; АМГ – антимюллеров гормон, IL-18 – интерлейкин (IL)-18, ССГ – секс-стероид-связывающий глобулин.
Notes: * – differences from group 1 at p < 0.05; AMH – anti-Müllerian hormone, IL-18 – interleukin (IL)-18, SSBG – sex-steroid-binding globulin.
Источник: таблица составлена авторами.
Source: the table is compiled by the authors.
Была установлена диагностическая ценность исследования сывороточных уровней предложенных параметров в аспекте прогнозирования результативности применения ВРТ. У количества АМГ в предложенном диапазоне определилась чувствительность (Se) – 70,6 %, специфичность (Sp) – 37,9 %; у IL-18 – Se 100 %, Sp 41,4 %; у ССГ – Se 29,4 %, Sp 93,1 %. В свою очередь, детекция комбинации АМГ, IL-18, ССГ относительно благоприятного исхода процедуры ВРТ показала Se 78,4 %, Sp 62,1 %.
Для подтверждения целесообразности применения способа приводим клинические примеры.
Пример 1. Больная Ш., 47 лет, поступила на обследование и лечение 05.09.2023 г. (на 2 день менструального цикла) с жалобами на отсутствие зачатия.
В анамнезе 3 беременности, 2 из которых закончились родами, 3-я – выкидышем. Отсутствие зачатия беспокоит в течение 3 лет. Индекс массы тела – 26,17 кг/м2.
После проведенного обследования выставлен диагноз: бесплодие женское, связанное с отсутствием овуляции. Рубец на матке после консервативной миомэктомии. Узловой зоб 1 степени. Эутиреоз.
УЗИ матки и придатков от 05.09.2023 г.: в обоих яичниках по 3–5 фолликулов размером по 2–3 мм, признаки аденомиоза.
УЗИ молочных желез от 05.09.2023 г.: признаки фиброзной диффузной левосторонней мастопатии.
Иммунологическое исследование от 06.09.2023 г.: количество AМГ – 1,3 нг/мл, IL-18 – 145 пг/мл, ССГ – 103 нмоль/л.
После проведения ЭКО зафиксировано наступление беременности, что полностью соответствовало прогнозируемому результату.
Пример 2. Больная Н., 31 год, поступила на обследование и лечение 11.12.2023 г. (на 3 день менструального цикла) с жалобами на отсутствие зачатия в течение 1 года.
В анамнезе беременность отсутствует, 1 протокол ЭКО с отрицательным результатом. Индекс массы тела – 31 кг/м2.
После проведенного обследования выставлен диагноз: бесплодие женское, связанное с отсутствием овуляции. Диффузная кистозная мастопатия. Ожирение 1 ст. Гиперхолестеринемия.
УЗИ матки и придатков от 11.12.2023 г.: в правом яичнике 7 фолликулов размером до 7 мм, в левом яичнике 5 фолликулов размером до 8 мм, признаки аденомиоза.
УЗИ молочных желез от 11.12.2023 г.: мелкая солитарная киста правой молочной железы.
Иммунологическое исследование от 12.12.2023 г.: количество AМГ – 10 нг/мл, IL-18 – 133 пг/мл, ССГ – 117 нмоль/л.
После проведения ЭКО зафиксировано наступление беременности, что полностью соответствовало прогнозируемому результату.
Пример 3. Больная А., 31 год, поступила на обследование и лечение 05.02.2024 г. (на 2 день менструального цикла) с жалобами на отсутствие зачатия.
В анамнезе 1 замершая беременность раннего срока, 3 протокола ЭКО с отрицательным результатом. Отсутствие зачатия беспокоит в течение 7 лет. Индекс массы тела – 27,71 кг/м2.
После проведенного обследования выставлен диагноз: бесплодие женское. Эндометриоз матки. Субклинический гипотиреоз в стадии медикаментозной компенсации. Диффузная кистозная мастопатия.
УЗИ матки и придатков от 05.02.2024 г.: в правом яичнике 12 фолликулов размером до 6 мм, в левом яичнике 10 фолликулов размером до 6 мм, признаки поликистозных яичников.
УЗИ молочных желез от 05.02.2024 г.: признаки мелких кистозных включений молочных желез.
Иммунологическое исследование от 06.02.2024 г.: количество AМГ –16,2 нг/мл, IL-18 – 325 пг/мл, ССГ – 19 нмоль/л.
После проведения ЭКО зафиксировано ненаступление беременности, что полностью соответствовало прогнозируемому результату.
Пример 4. Больная П., 35 лет, поступила на обследование и лечение 18.03.2024 г. (на 2 день менструального цикла) с жалобами на отсутствие зачатия.
В анамнезе беременность отсутствует, двусторонний гидросальпинкс, гиперплазия эндометрия, 2 протокола ЭКО с отрицательным результатом. Отсутствие зачатия беспокоит в течение 5 лет. Индекс массы тела – 23,37 кг/м2.
После проведенного обследования выставлен диагноз: бесплодие женское, трубно-перитонеального генеза. Фиброаденома левой молочной железы.
УЗИ матки и придатков от 18.03.2024 г.: в правом яичнике 8 фолликулов размером до 7 мм, в левом яичнике 10 фолликулов размером до 7 мм, признаки диффузных изменений структуры матки по типу эндометриоза.
УЗИ молочных желез от 18.03.2024 г.: фиброаденома левой молочной железы.
Иммунологическое исследование от 19.03.2024 г.: количество AМГ –1,15 нг/мл, IL-18 – 183 пг/мл, ССГ – 29 нмоль/л.
После проведения ЭКО зафиксировано ненаступление беременности, что полностью соответствовало прогнозируемому результату.
ОБСУЖДЕНИЕ И ЗАКЛЮЧЕНИЕ
Разработанный способ иммунологического прогнозирования эффективности применения ВРТ предусматривает сочетанное определение в сыворотке крови количества АМГ, IL-18 и ССГ для предикции благоприятного исхода применения ВРТ. Успешная апробация способа в когорте женщин с первичным бесплодием указывает на возможность использования способа для иммунодиагностики, прогнозирования исхода процедуры ВРТ, улучшения демографических показателей. Применение способа может способствовать персонализированному определению шансов наступления беременности и оценке целесообразности проведения ЭКО, оптимизации тактики ведения пациенток.
1 ВОЗ. Бесплодие. Информационный бюллетень. URL: https://www.who.int/ru/news-room/fact-sheets/detail/infertility (дата обращения: 05.09.2025).
About the authors
Anastasia S. Andreeva
National Research Mordovia State University
Email: galynia.a@yandex.ru
ORCID iD: 0009-0001-6059-5689
Postgraduate Student, Department of Immunology, Microbiology, and Virology with a course in Clinical Immunology and Allergology, Institute of Medicine
68 Bolshevistskaya St., Saransk 430005, Russian FederationLyubov V. Matveeva
National Research Mordovia State University
Author for correspondence.
Email: Matveevaljubov1@mail.ru
ORCID iD: 0000-0001-9342-3157
SPIN-code: 6017-0118
Scopus Author ID: 55257966400
Dr.Sci. (Med.), Associate Professor of the Department of Immunology, Microbiology and Virology with a course in Clinical Immunology and Allergology, Institute of Medicine
68 Bolshevistskaya St., Saransk 430005, Russian FederationAlena I. Adamchik
Mordovia Republican Central Clinical Hospital
Email: perinatrm@mail.ru
ORCID iD: 0009-0004-6247-556X
Cand.Sci. (Med.), Head of the Assisted Reproductive Technologies Department, Perinatal Center
18 Pobedy St., Saransk 430005, Russian FederationOlga V. Epifanova
Mordovia Republican Central Clinical Hospital
Email: epifanova.vrt@gmail.com
ORCID iD: 0000-0002-3961-809X
Cand.Sci. (Med.), Obstetrician-Gynecologist, Perinatal Center
18 Pobedy St., Saransk 430005, Russian FederationTatyana E. Chestnova
Mordovia Republican Central Clinical Hospital
Email: chestnova2022@gmail.com
ORCID iD: 0009-0005-6635-050X
Obstetrician-Gynecologist, Perinatal Center
18 Pobedy St., Saransk 430005, Russian FederationReferences
- Ozcan P., Takmaz T. Identification of Predictive Factors for the Probability of Pregnancy Following Ovulation Stimulation-intra-uterine Insemination Cycles in Terms of Female and Male. The Journal of Obstetrics and Gynaecology Research. 2021;47(3):893–899. https://doi.org/10.1111/jog.14594
- Zheleznaya A.A., Myagkikh I.I. Features of the Somatic Anamnesis of Women of Late Reproductive Age Suffering From Infertility. Bulletin of Urgent and Recovery Surgery. 2021;6(4):63–68. https://elibrary.ru/fzlbrg
- Andreeva A.S., Matveeva L.V., Fominova G.V. Method for Immunological Prediction of Effectiveness of Using Assisted Reproductive Technologies. Patent 2836007 C1 Russian Federation. March 10, 2025. https://elibrary.ru/kstrri
Supplementary files